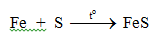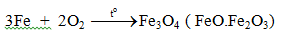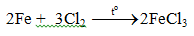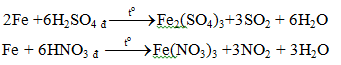Sắt là kim loại được ứng dụng rất nhiều trong thực tế, nhưng có thể bạn chưa biết tính chất hóa học và tính chất vật lý của Sắt. Để tìm hiểu các ứng dung của Sắt và tính chất hóa học của Sắt mời các em cùng theo dõi ở bài viết sau đây.
Định nghĩa Sắt.
Sắt là một kim loại phổ biến trên bề mặt Trái Đất, là một trong những nguyên tố hóa học quan trọng trong bảng tuần hoàn các nguyên tố hóa học, ký hiệu của sắt là Fe với số hiệu nguyên tử là 56, sắt là kim loại đứng sau nhôm và đứng trước Cr trong phân nhóm VIIIB chu kỳ thứ tư.
Tính chất vật lý của Sắt
– Sắt là kim loại có màu trắng hơi xám, dẻo, dễ rèn, nóng chảy ở nhiệt độ 1540ºC, có D = 7,9 g/cm3.
– Sắt có tính dẫn điện, dẫn nhiệt tốt, đặc biệt có tính nhiễm từ (bị nam châm hút và sắt cũng có thể nhiễm từ trở thành nam châm).
– Khối lượng riêng D = 7,86g/cm³, nóng chảy ở 1539°c. Sắt dẻo nên dễ rèn.
Tính chất hóa học của Sắt
– Sắt là kim loại có tính khử trung bình, tùy theo các chất oxi hóa mà sắt có thể bị oxi hóa lên mức +2 hay +3.
Fe → Fe2+ + 2e
Fe → Fe3+ + 3e
Fe tác dụng với phi kim
- Tác dụng với lưu huỳnh
- Tác dụng với oxi
- Tác dụng với clo
Fe tác dụng với axit
- Tác dụng với dung dịch axit HCl, H2SO4 loãng
Fe + 2H+ → Fe2+ + H2
- Tác dụng với các axit HNO3, H2SO4 đặc
Fe + 4HNO3 l → Fe(NO3)3 + NO + 2H2O
Chú ý: Với HNO3 đặc, nguội; H2SO4 đặc, nguội: Fe bị thụ động hóa.
Fe tác dụng với dung dịch muối
– Fe đẩy được kim loại đứng sau ra khỏi dung dịch muối của chúng:
Fe+ CuSO4 → FeSO4 + Cu
Chú ý:
Fe + 2Ag+ → Fe2+ + 2Ag
Ag+ dư + Fe2+ → Fe3+ + Ag
- Xem thêm : Tính chất hóa học của Đồng
Ứng dụng của sắt
Sắt có tính ứng dụng vô cùng cao và nó chiếm đến 95% tổng khối lượng được sản xuất ra hàng năm trên thế giới. Một số ứng dụng phổ biến của sắt như sau:
- Tham gia phản ứng đúc gàn, trong đó nổi bật là gang thô. Fe là chất trung gian trong các phản ứng. Gang thô có đặc tính là rất rắn, cứng và dễ vỡ nhưng lại được ứng dụng phổ biến.
- Sản xuất ra thép cacbon cùng với lượng nhỏ các chất khác như P, Si, Mn, S…
- Sản xuất sắt non, có đặc tính dai và dễ uốn, vì hàm lượng caascbon ít nên rất dễ mài và sắc bén.
- Sản xuất ra thép hợp kim.
- Oxit sắt III có tác dụng là chất tạo nên các bộ lưu từ trong máy tính và được trộn lẫn với một số chất khác.
- Sắt Sunfat là một thành phần tạo nên xi măng.