Trong tính chất hóa học của Bazo bạn sẽ thấy oxit bazo tác dụng với nước, bài viết này sẽ làm rõ hơn kiến thức khi cho oxit bazơ tác dụng với nước có phương trình phản ứng và bài tập ví dụ đi kèm.
- Xem thêm : Oxit Axit tác dụng với Bazo
PTPU Oxit Bazơ tác dụng với Nước
+ Một số Oxit bazo tác dụng với nước tạo thành dung dịch bazo (kiềm)
PTPƯ: Oxit bazo + H2O → Bazo
BaO(r) + H2O (dd) → Ba(OH)2,(dd)
K2O + H2O (dd) → 2KOH
BaO + H2O (dd) → Ba(OH)2
+ Một số oxit bazo khác tác dụng với nước như: K2O, Li2O, Rb2O, Cs2O, SrO,…
+ Dung dịch bazơ làm đổi màu quỳ tím thành xanh.
- Xem thêm : Oxit axit là gì
Bài tập tính khi cho nước tác dụng với oxit bazo
Bài 1 : Oxit bazơ nào sau đây không tác dụng với nước:
A. BaO
B. Na2O
C. CaO
D. Al2O3
Lời giải
Nước có thể tác dụng với một số oxit bazơ như K2O, Na2O, CaO, BaO … tạo ra bazơ ⇒ Oxit bazơ không tác dụng với nước là: Al2O3.
⇒ Đáp án : D
Bài 2 : Cho 12,4 gam natri oxit tác dụng hết với nước.
a) Viết phương trình hóa học.
b) Tính khối lượng natri hiđroxit có trong dung dịch thu được.
Lời giải
a) Phương trình hóa học: Na2O + H2O → 2NaOH
b) Số mol Na là: nNa2O = 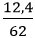
Na2O + H2O → 2NaOH
0,2 → 0,4 (mol)
Theo phương trình: nNaOH = 2nNa2O = 0,4 mol
Khối lượng natri hiđroxit có trong dung dịch thu được là:
mNaOH = nNaOH.MNaOH = 0,4.40 = 16 gam
Bài 3 :
Hòa tan hỗn hợp gồm (28,4 gam P2O5 và 12 gam SO3) vào nước dư, thu được dung dịch chứa bao nhiêu gam chất tan?
Lời giải
Số mol P2O5 là: nP2O5 = 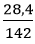
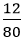
Phương trình hóa học:
P2O5 + 3H2O → 2H3PO4
0,2 → 0,4 (mol)
Khối lượng H3PO4 là: mH3PO4 = nH3PO4.MH3PO4 = 0,4.98 = 39,2 gam
SO3 + H2O → H2SO4
0,15 → 0,15 (mol)
Khối lượng H2SO4 là: mH2SO4 = nH2SO4.MH2SO4 = 0,15.98 = 14,7 gam
Tổng khối lượng H3PO4 và H2SO4 có trong dung dịch thu được là:
mhh = 39,2 + 14,7 = 53,9 gam.
