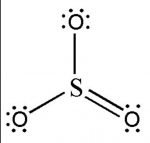
Công thức hóa học SO3 các bạn sẽ gặp khá nhiều trong các bài tập hóa học tính hóa trị của gốc axit này! Như vậy SO3 hóa trị mấy? SO3 là oxit gì?Bài viết này sẽ làm rõ hóa trị của gốc SO3 lưu huỳnh Trioxit.
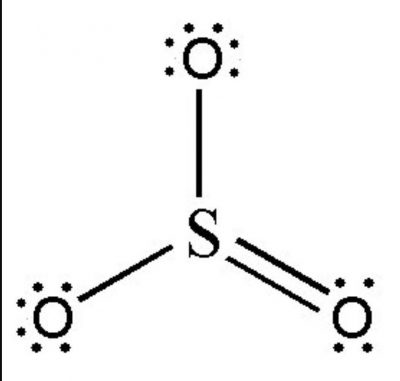
SO3 là gì?
SO3 là lưu huỳnh trioxit, Điều kiện thường, SO3 là chất lỏng, không màu.
– Nhiệt độ nóng chảy: 17ºC; nhiệt độ sôi: 45ºC.
– Tan vô hạn trong nước và trong axit H2SO4
Tính chất hóa học
SO3 là 1 oxit axit
SO3 tác dụng với nước → dung dịch axit
SO3 + H2O → H2SO4
Chú ý: H2SO4 là 1 axit mạnh và có tính oxi hóa mạnh.
SO3 tác dụng với dung dịch bazơ có thể tạo thành 2 loại muối sunfat và hiđrosunfat
SO3 + KOH → KHSO4
SO3 + 2KOH → K2SO4 + H2O
SO3 + NaOH → có thể tạo 2 muối: muối axit hiđrosunfat (chứa ion HSO4-); muối trung hòa sunfat (chứa ion SO42-) tùy tỉ lệ.
SO3 tác dụng với oxit bazơ → muối
SO3 + BaO → BaSO4
SO3 hóa trị mấy? Oxit gì?
SO3 nằm trong nhóm nguyên tử có hóa trị II: =S, =SO3, =SO4, =HPO4, =HPO3, =SiO3
SO3 là oxit axit : tác dụng với nước cho sản phẩm là axit và tác dụng với bazo cho sản phẩm là muối
Tác dụng với H2O tạo axit sunfuric: SO3 + H2O → H2SO4
SO3 tan vô hạn trong H2SO4 tạo oleum H2SO4.nSO3
Tác dụng với bazo tạo muối : SO3 + 2NaOH → Na2SO4 + H2O