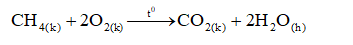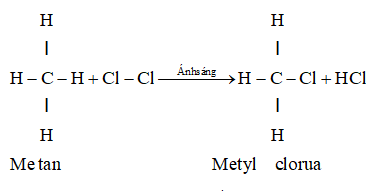Công thức hóa học CH4 chắc chắn các bạn phải gặp rất nhiều trong các bài tập hoặc các phương trình hóa học. Ch4 là gì? Các tính chất và ứng dụng của CH4 như thế nào? Mời các bạn cùng theo dõi bài viết sau đây.
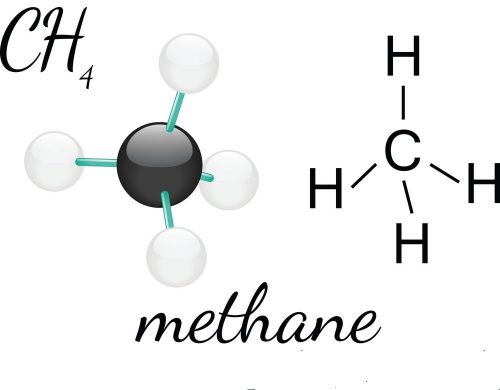
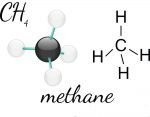
CH4 là gì?
Ch4 là công thức hóa học của khí Metan, Nó là một hydrocacbon nằm trong dãy đồng đẳng Ankan. Metan là trong tự nhiên tồn tại trong bùn ao, khí đầm lấy, trong dầu mỡ là khí dầu mỡ hay khí đồng hành, trong mỏ than là khí than, trong hầm biogas còn gọi là khí Biogas.
Tính chất vật lí của CH4
Metan là chất khí không màu, không mùi, không vị. Là khí rất độc. Đặc biệt dễ bắt cháy, khi cháy tạo ra lửa màu xanh.
- Khối lượng riêng của metan là 0.717 kg/m3‑, nhẹ hơn không khí
- CH4 hóa lỏng khi ở −162 °C, hóa rắn ở −183 °C
- Điểm bốc cháy là 537 °C
- Khí metan hòa tan tốt trong dung môi không phân cực. Còn đối với dung môi phân cực thì nó không có khả năng hòa tan vì không có sự liên kết.
- CH4 không có tính dẫn điện.
Tính chất hóa học của Metan và ứng dụng của Metan.
Ch4 tác dụng với oxi
-Metan cháy tạo thành khí cacbon đioxit và hơi nước.
Phản ứng trên tỏa nhiều nhiệt. Hỗn hợp gồm một thể tích metan và hai thể tích oxi là hỗn hợp nổ mạnh.
Ch4 tác dụng với Clo
Metan tác dụng với clo khi có ánh sáng.
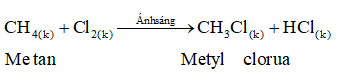
Viết gọn:
Phản ứng trên, nguyên tử hidro của metan được thay thế bởi nguyên tử clo. Vì vậy phản ứng trên được gọi là phản ứng thế.
Ch4 phản ứng nhiệt phân
2CH4 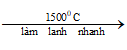
Ứng dụng của Metan
Metan có 2 ứng dụng lớn là:
Ứng dụng CH4 làm các nhiên liệu
CH4 cũng chính là một nhiên liệu không thể thiếu trong đời sống, đặc biệt có trong khí gas. Nấu bằng khí gas, đồ sưởi ấm giúp bạn giảm bớt lượng thải CO, CO2 ra ngoài không khí thay vì dùng bằng than, củi.
Ứng dụng CH4 vào công nghiệp
Metan khá tích cực trong các phản ứng hóa học ở nhiều dạng khác nhau: rắn, lỏng, khí. Trong các ngành công nghiệp hóa học, metan là nguyên liệu tạo ra một số chất như hydro, methanol, axit axetic và anhydrit axetic.