Cho kẽm ký hiệu là Zn tác dụng với Hno3 ta thu được những chất gì? Cùng xem phương trình và cân bằng phương trình phản ứng giữa Zn + Hno3 tại đây nhé!
- Xem thêm : Na2co3 + H2so4
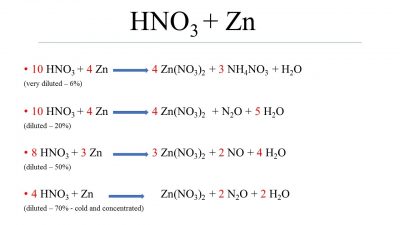
Zn + Hno3 phương trình phản ứng.
10Hno3 + 4Zn → 3h2O + Nh4no3 + 4Zn(No3)2
| 10HNO3 | + | 4Zn | → | 3H2O | + | NH4NO3 | + | 4Zn(NO3)2 |
| axit nitric | kẽm | nước | amoni nitrat | Kẽm nitrat | ||||
| (dd) | (rắn) | (lỏng) | (rắn) | |||||
| (không màu) | (ánh kim bạc xám) | (không màu) | (trắng) |
- Bạn có thể quan tâm : Nano3 ra hno3
Zn tác dụng HNO3 loãng
Cho Zn tác dụng với axit nitric loãng
3Zn + 8HNO3 → 3Zn(NO3)2 + 2NO + 4H2O
Zn tác dụng HNO3 Đặc
Cho Zn ( kẽm ) phản ứng với axit nitric đặc
Zn + 4HNO3 → 3Zn(NO3)2 + 2NO + 2H2O
Bài tập ví dụ có Zn và Hno3
Ví dụ 1 : Hợp chất nào sau đây không có tính lưỡng tính?
A. ZnO
B. Zn(OH)2
C. ZnSO4
D. Zn(HCO3)2
Lời giải
Chọn đáp án : C
Ví dụ 2: Cho 6,5 gam Zn tác dụng với HNO3 dư thu được V lít NO2 (đktc) là sản phẩm khử duy nhất. Giá trị của V là
A. 2,24
B. 3,36
C. 4,48
D. 6,72
Zn → Zn+2 + 2e
0,1 0,2
N+5 + 1e → N+4
x x
Bảo toàn electron ne cho= ne nhận
=> x = 0,2
=> V= 0,2.22,4=4,48 lít
Chọn đáp án : C
Ví dụ 3 : X là hợp chất của Zn được dùng trong y học với tác dụng làm thuốc giảm đau dây thần kinh, chữa bệnh eczema, bệnh ngứa,…Chất X là:
A. ZnO
B. ZnSO4
C. Zn(OH)2
D. Zn(NO3)2
Lời giải
Chọn đáp án A
Ví dụ 4 : Cho 11 g hỗn hợp hai kim loại Al và Fe vào dung dịch HNO3 loãng dư, thu được 6,72 lit khí NO (đktc) duy nhất. Khối lượng (g) Fe trong hỗn hợp đầu?
A. 5,6 gam
B. 2,8 gam
C. 8,4 gam
D. 4,2 gam
Lời giải
nNO = 6,72/22,4 = 0,3 mol
N+5 + 3e → N+2
Gọi x, y lần lượt là số mol Al và Fe trong hỗn hợp đầu
Ta có: 27x + 56y = 11 (1)
Al → Al+3 + 3e
x mol 3x mol
Fe → Fe+3 + 3e
y mol 3y mol
Theo định luật bảo toàn e: ne (KL nhường) = ne (N nhận) = 0,9 mol
hay: 3x + 3y = 0,9 (2)
Từ (1) và (2) ta có x = 0,2; y = 0,1 => mAl= 5,4; mFe = 5,6 gam

