Bạn đang muốn tìm lời giải cho công thức hóa học NH3, NH3 là Gì? NH3 là liên kết gì, chất gì, có tính gì…? Đây là những câu hỏi phổ biến về công thức hóa học này. Để giải đáp được những câu hỏi về NH3 mời các bạn cùng theo dõi đầy đủ tính chất hóa học của NH3 ở bài viết này nhé!
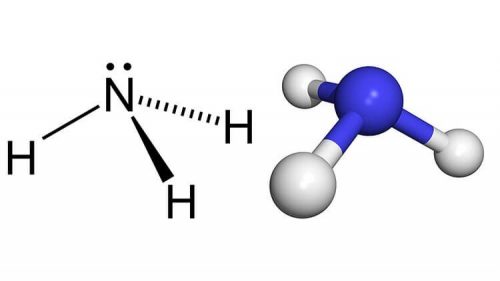
NH3 là gì? Liên kết gì?
NH3 là công thức hóa học của Amoniac. Ở nhiệt độ bình thường, đây là khí độc, khí có mùi khai. Amoniac lỏng là một hợp chất vô cơ, Amoniac lỏng công nghiệp thường là 28% NH3 trong nước và được chứa trong bình chứa.
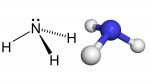
NH3 là hợp chất được cấu tạo từ ba nguyên tử hidro liên kết hóa học với một nguyên tử nitơ trung tâm, có nguồn gốc từ các nguồn tự nhiên cũng như tổng hợp công nghiệp. NH3 là một loại khí không màu dễ tan trong nước và hóa lỏng. Ở trạng thái lỏng nó có thể được sử dụng làm chất làm lạnh.
Tính chất vật lý của NH3.
Amoniac (NH3) thường tồn tại ở dạng khí, không màu, có mùi hôi hay hăng khó chịu. Nồng độ Amoniac lớn có thể gây chết người.
Khối lượng phân tử tương đối: 17.031 g/mol
Mật độ amoniac trong điều kiện tiêu chuẩn là 0,771g / L
Điểm nóng chảy: -77,7 oC
Điểm sôi: -33,5 oC
Độ hòa tan: dễ dàng hòa tan trong nước (1: 700)
Mật độ tương đối trong nước: 0,82 (-79 ℃)
Mật độ tương đối trong không khí: 0,5971
Amoniac có độ phân cực lớn do phân tử NH3 có cặp electron tự do và liên kết N–H bị phân cực. Do đó NH3 là chất dễ hoá lỏng.
Dung dịch Amoniac là dung môi hoà tan tốt: NH3 hoà tan các dung môi hữu cơ dễ hơn nước do có hằng số điện môi nhỏ hơn nước. Kim loại kiềm và các kim loại Ca, Sr, Ba có thể hòa tan trong NH3 lỏng tạo dung dịch xanh thẫm.
Tính chất hóa học của NH3.
NH3 có tính bazơ yếu
NH3 có tính bazơ nên khí amoniac làm giấy quỳ tím chuyển sang màu xanh và có đầy đủ tính chất hóa học của một dung dịch kiềm nên nó có thể tác dụng với axit, kim loại, muối…
NH3 tác dụng với axit
NH3 tác dụng với axit nhưng sản phẩm thu được thường là muối amoni axit tương ứng và nước.
H2SO4 + 2NH3 → (NH4)2SO4
NH3 + HCl → NH4Cl
HNO3 + 3NH3 → 2NH4NO + H2O
NH3 tác dụng với oxit axit
Khí NH3 dễ dàng tác dụng với nhiều oxit axit hoạt động mạnh và yếu.
NH3 tác dụng với oxit axit
NH3 + CuO -> Cu + H2O + N2
2NH3 + 2CrO3 → 3H2O + N2 + Cr2O3
NH3 tác dụng với muối
Khí amoniac tác dụng với muối để tạo thành bazơ mới và muối mới với chất xúc tác thường là nước.
NH3 + H2O + CuSO4 → (NH4)2SO4 + Cu(OH)2 ↓
2NH3 + AlCl3 + 2 H2O -> Al(OH)3 + 2NH4Cl
NH3 tác dụng với phi kim ( Phản ứng oxy hóa)
Vì phân tử nitơ là chất oxy hóa nên NH3 có tính khử mạnh khi tác dụng với nhóm halogen như clo và oxy.
2NH3 + 3Cl2 -> N2 + 6HCl ( đk là nhiệt độ cao)
8NH3 + 3Cl2 -> N2 + 6NH4Cl
4NH3 + 5O2 → 6H2O + 4NO ( điều kiện 800°C)
4NH3 + 7O2 → 4NO2 + 6H2O
4NH3 + 3O2 → 2N2 + 6H2O ( điều kiện 500°C)
NH3 tác dụng với kim loại
NH3 Có thể tác dụng với nhóm kim loại kiềm và nhôm.
2NH3 + 2Na → 2NaNH2 + H2 (350 °C)
2K + 2NH3 → H2 + 2KNH2 (khí)
2NH3 + 2Al → 2AlN + 3H2
Cách nhận biết Nh3 (Amoniac)
Amoniac có tính bazơ nên dung dịch NH3 làm cho quỳ tím hóa xanh còn dung dịch phenolphtalein từ màu chuyển thành hồng. Do đó để phát hiện Amoniac, người ta dùng quỳ tím ẩm để nhận biết.