Học bảng tuần hoàn nguyên tố hóa học có thể nói khá khó khăn với học sinh, để thuộc hết các nguyên tố trong bảng tuần hoàn này các em cần phải bỏ nhiều thời gian hơn nhưng cũng có một số mẹo nhỏ để các em có thể thuộc được bảng nguyên tố hóa học dễ dàng hơn. Dưới đây là bảng tuần hoàn nguyên tố hóa học đầy đủ nhất cho bạn nhé!
Bạn cần biết : Bảng hóa trị đầy đủ
Bảng tuần hoàn các nguyên tố hóa học đầy đủ.
Bảng tuần hoàn hóa học được sử dụng trong thời điểm hiện nay đã được chỉnh sửa và mở rộng thêm vì sự phát hiện các nguyên tố mới khác. Tuy nhiên, về mặt hình thức thì bảng tuần hoàn các nguyên tố hóa học hiện tại vẫn giữ được đúng những nét cơ bản của bảng tuần hoàn gốc của Mendeleev.
Các nguyên tố hóa học là chất hóa học tinh khiết được phân biệt bới số hiệu nguyên tử hay gọi là số proton có trong mỗi hạt nhân. Để dễ học bảng tuần hoàn hóa học người ta đã sắp xếp theo thứ tự các số hiệu nguyên tử tăng dần cảu các nguyên tố và hiển thị với các ký hiệu tương ứng ở mỗi ô như hình ảnh dưới đây để các em tiện theo dõi.
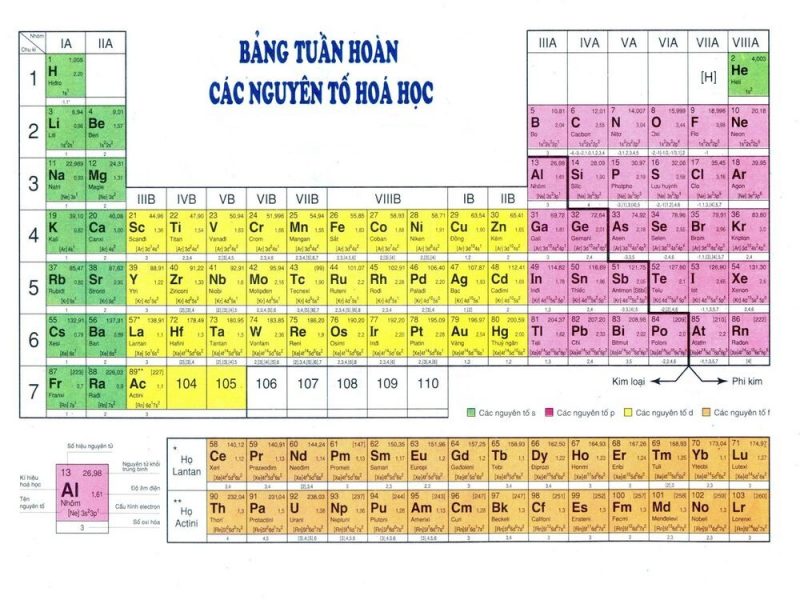
Cách đọc bảng nguyên tố hóa học
1) Số nguyên tử: Hay còn gọi là số proton của 1 nguyên tố hóa học là số proton được tìm thấy trong hạt nhân của 1 nguyên tử. Là số điện tích của hạt nhân. Số nguyên tử giúp xác định duy nhất một nguyên tố hóa học. Số nguyên tử cũng bằng số electron trong một nguyên tử trung hòa về điện.
2) Nguyên tử khối trung bình: Gần như các nguyên tố hóa học là hỗn hợp của nhiều đồng vị với tỉ lệ phần trăm số nguyên tử xác định. Nên nguyên tử khối của các nguyên tố có nhiều đồng vị là nguyên tử khối trung bình của hỗn hợp các đồng vị có tính đến tỉ lệ phần trăm số nguyên tử tương ứng.
3) Độ âm điện: Độ âm điện của 1 nguyên tử là khả năng hút electron của nguyên tử đó khi tạo thành liên kết hóa học. Quy tắc: Độ âm điện của nguyên tử nguyên tố càng lớn thì tính phi kim nguyên tố đó càng mạnh và ngược lại.
4) Cấu hình electron: Cấu hình electron nguyên tử cho biết sự phân bố các electron trong lớp vỏ nguyên tử ở các trạng thái năng lượng khác nhau hay ở các vùng hiện diện của chúng.
5) Số oxi hóa: Là số áp cho một nguyên tử hay nhóm nguyên tử. Nhờ số oxi hóa, chúng ta có thể nhận biết được số electron trao đổi khi một chất bị oxi hóa hoặc bị khử trong một phản ứng.
6) Tên nguyên tố: Là 1 chất hóa học tinh khiết, bao gồm 1 kiểu nguyên tử, được phân biệt bởi số hiệu nguyên tử, là số lượng proton có trong mỗi hạt nhân.
7) Ký hiệu hóa học: Trong hóa học, ký hiệu là tên viết tắt của một nguyên tố hóa học đó. Biểu tượng cho các nguyên tố hóa học thường bao gồm 1 hoặc 2 chữ cái trong bảng chữ cái Latin và được viết với chữ cái đầu tiên viết hoa.
Cách sắp xếp các nguyên tố trong bảng tuần hoàn.
Xem thêm : Bảng nguyên tử khối hóa học
Sắp xếp theo nhóm
Các nguyên tố xếp chung một nhóm sẽ có cấu hình electron như nhau trong lớp hóa trị và do đó các nguyên tố này sẽ có tính chất hóa học tương tự nhau. Trong một nhóm, số hiệu nguyên tử và bán kính của các nguyên tố sẽ tăng dần từ trên xuống dưới. Do đó, mức năng lượng của các nguyên tử sẽ được lấp đầy hơn, các electron ngoài cùng cũng sẽ cách xa hạt nhân hơn.
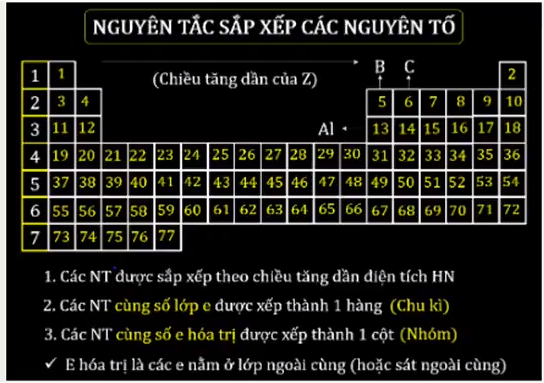
Sắp xếp các nguyên tố theo chu kỳ
Các nguyên tố được sắp theo chu kỳ nghĩa là được sắp xếp thành một hàng ngang trong bảng tuần hoàn. Theo chiều từ trái sang phải, bán kính nguyên tử của nguyên tố sẽ giảm dần còn độ âm điện và năng lượng ion hóa sẽ tăng dần do sự tăng dần của số proton trong hạt nhân sẽ làm cho e lớp ngoài cùng được kéo lại gần hơn.
Hiện tại bảng tuần hoàn nguyên tố hóa học gồm có 7 chu kỳ: Chu kỳ 1, 2 và 3 được gọi là chu kỳ nhỏ. Chu kỳ 4,5,6 và 7 được gọi là chu kỳ lớn.
Chu kỳ 1: có 2 nguyên tố là Hidro ( Z=1) và Heli (Z=2).
Chu kỳ 2: có 8 nguyên tố từ Liti (Z=3) đến Neon (Z=10).
Chu kỳ 3: có 8 nguyên tố từ Natri (Z=11) đến Argon (Z=18).
Chu kỳ 4: có 18 nguyên tố từ Kali (Z=19) đến Krypton (Z=36).
Chu kỳ 5: có 18 nguyên tố từ Rubidi (Z=37) đến Xenon (Z=54).
Chu kỳ 6: có 32 nguyên tố từ Xesi (Z=55) đến Ranon (Z=86).
Chu kỳ 7: bắt đầu từ nguyên tố Franxi (Z=87) đến nguyên tố Z=110.
Sắp xếp theo phân nhóm
Có thể xếp các nguyên tố trong bảng tuần hoàn các nguyên tố hóa học vào 4 phân nhóm khác nhau là s, p, d và f. Theo IUPAC, electron cuối cùng của nguyên tử nguyên tố được điền vào phân lớp nào (theo trình tự mức năng lượng) thì nguyên tố đó sẽ thuộc phân nhóm đó.
Trên đây là toàn bộ bảng tuần hoàn hóa học mà học sinh bắt buộc phải nhớ nếu muốn học tốt môn hóa học. Bảng tuần hoàn này sẽ theo các em xuyên suốt trong trương trình thcs, thpt và chương trình đại học đó nhé!

