axitnitric là gì?
Axit nitric là một hợp chất hữu cơ có tên gọi hóa học chung đó là HNO3. Ở dạng chất lỏng, HNO3 thường không có màu và có bốc khói mạnh trong không khí có độ ẩm. Ở tự nhiên Axit Nitric được cấu thành và tạo ra từ những đợt sấm chớp và mưa sét. Cho đến hiện đại theo các chứng minh khoa học thì HNO3 là một tác nhân gây ra các trận mưa Axit hủy diệt.
Chính vì sự đặc biệt này nên HNO3 luôn là một hợp chất hóa học có tính sát thương và nguy hiểm cao. Nó là một chất axit cực độc, dễ ăn mòn và dễ tạo ra cháy nổ có tính sát thương cũng cực kỳ cao. Ngoài thực tế HNO3 không màu, ở dạng tinh khiết, nếu như bạn để lâu thì HNO3 sẽ bị chuyển sang màu vàng.
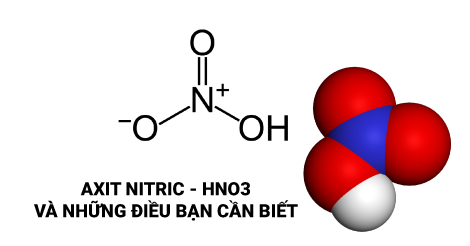
Công thức hóa học của axitnitric
Axit nitric có công thức hóa học là HNO3, được gọi là dung dịch nitrat hidro hay còn được gọi là axit nitric khan. Axit này được hình thành ở trong tự nhiên, tạo ra từ những cơn mưa do sấm và sét tạo thành.
Axit nitric HNO3 tạo thành từ 1 nguyên tử hidro và 1 gốc nitrat NO3-, tạo ra từ sự hòa tan của khí nito dioxit (NO2) trong nước dưới sự có mặt của khí oxi
4NO2 + O2 + 2H2O → 4HNO3
Tính chất của Axit nitric hno3
Đặc tính vật lý của axitnitric
- Công thức hóa học: H N O 3
- Khối lượng phân tử chính: 63.012 g · mol −1
- Ngoại quan: Chất lỏng bốc khói không màu, vàng hoặc đỏ
- Mùi: vị chát, ngột ngạt
- Tỉ trọng: 1,51 g cm 3 , 1,41 g cm 3 [68% w / w]
- Độ nóng chảy: −42 ° C (−44 ° F; 231 K)
- Điểm sôi: 83 ° C (181 ° F; 356 K) dung dịch 68% sôi ở 121 ° C (250 ° F; 394 K)
- Độ hòa tan trong nước: Hoàn toàn có thể trộn được
- Đăng nhập P: .130,13
- Áp suất hơi: 48 mmHg (20 ° C)
- Độ Axit: −1.4
- Cơ sở liên hợp: Nitrat
- Nhạy cảm từ: 1,99 × 10 −5 cm 3 / mol
- Chỉ số khúc xạ: 1.394 (16,5 ° C)
- Khoảnh khắc lưỡng cực: 2,17 ± 0,02 D
Tính chất HNO3 là một axit mạnh
Làm quỳ tím chuyển thành màu đỏ.
Tác dụng với oxit bazơ (trong đó kim loại đã đạt hóa trị cao nhất) → muối + H2O
Tác dụng với bazơ (trong đó kim loại đã đạt hóa trị cao nhất) → muối + H2O
2HNO3 + Mg(OH)2 → Mg(NO3)2 + 2H2O
Tác dụng với muối (trong muối kim loại đã đạt hóa trị cao nhất) → muối mới + axit mới
Tính chất HNO3 là chất oxi hóa mạnh
Tác dụng với kim loại:
Tác dụng với phi kim → NO2 + H2O + oxit của phi kim.
HNO3 phản ứng với hầu hết các kim loại trừ Au và Pt → muối nitrat + H2O và sản phẩm khử của N+5 (NO2, NO, N2O, N2 và NH4NO3). Sản phẩm khử của N+5 là tùy thuộc vào độ mạnh của kim loại và nồng độ của dung dịch axit. Thông thường thì dung dịch đặc → NO2, dung dịch loãng → NO; dung dịch axit càng loãng, kim loại càng mạnh thì N bị khử xuống mức càng sâu.