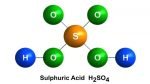
Các công thức hóa học hoặc bài tập môn hóa học các sẽ thường xuyên gặp các công thức H2SO4 đặc hay H2SO4 loãng? Như vậy thì H2SO4 là gì? Để biết rõ hơn về Công thức hóa học H2SO4 mời các bạn xem đầy đủ ở bài biết hôm nay nhé!
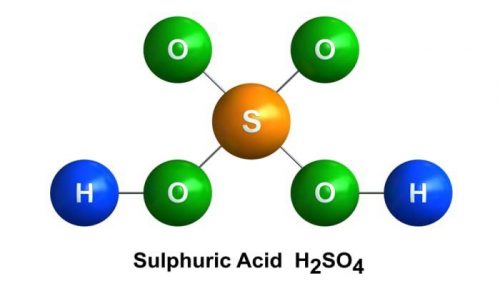
H2SO4 là gì?
H2SO4 là công thức hóa học của Axit Sunfuric. là một chất lỏng sánh như dầu, không màu, không mùi, không bay hơi, nặng gần gấp 2 lần nước (H2SO4 98% có D = 1,84 g/cm3). H2SO4 là một axit vô cơ mạnh và khả năng hòa tan hoàn toàn trong nước theo bất kỳ tỷ lệ nào.
Các loại Axit Sunfuric
Axit sunfuric được sử dụng với những mục đích khác nhau vì vậy nó sẽ được điều chế để phù hợp với mục đích sử dụng.
- Axit sunfuric loãng dùng trong phòng thí nghiệm thường chỉ có 10%.
- H2SO4 dùng cho ắc quy khoảng 33,5%.
- H2SO4 hàm lượng 62,18% là axit được dùng để sản xuất phân bón.
- H2SO4 77,67% được dùng trong tháp sản xuất hay axit glover.
- H2SO4 98% là axit đậm đặc.
Tính chất hóa học và Cách điều chế của Axit Sunfuric
H2SO4 có những tính chất hóa học chung của axit gồm:
+ Axit sulfuric là một axit mạnh và có tính ion hóa cao.
+ Hóa chất này có tính ăn mòn cao, phản ứng và hòa tan trong nước. Nó có khả năng oxy hóa rất cao và do đó, hoạt động như một tác nhân oxy hóa mạnh.
+ Nó có độ biến động rất thấp. Vì lý do này, nó đóng một phần trong việc điều chế các axit dễ bay hơi hơn từ các muối aixt khác.
+ Axit sulfuric đậm đặc là một chất khử nước rất mạnh. Do đó, hóa chất này được sử dụng để làm khô nhiều loại khí không phản ứng với axit.
+ Nó có khả năng làm mất nước các chất hữu cơ như tinh bột.
+ Nó có thể oxy hóa cả phi kim cũng như kim loại.
Tính chất khử nước của H2SO4 đậm đặc
Mất nước đề cập đến quá trình axit sunfuric đậm đặc loại bỏ các phân tử nước không tự do hoặc loại bỏ các nguyên tố hydro và oxy trong chất hữu cơ theo tỷ lệ thành phần nguyên tử hydro và oxy của nước.
Phản ứng tỏa nhiệt của Saccarozo dưới tác dụng của H2SO4
C12H22O11 + H2SO4 -> 12C + 11H2O
Phản ứng với cacbon tạo thành khí CO2, lưu huỳnh điôxít và nước.
C + H2SO4 -> CO2↑ + 2SO2 ↑ + 2H2O
Phản ứng oxi hóa mạnh
Vì là axit mạnh nên H2SO4 có khả năng phản ứng oxi hóa khử với nhiều chất, hợp chất khác nhau. Tùy vào chất khử, axit sunfuric đậm đặc có thể bị khử thành SO2, S hoặc H2S:
2HBr + H2SO4 (đậm đặc) = Br2 + SO2 + 2H2O
3H2S + H2SO4 (đậm đặc) = 4S + 4H2O
8HI + H2SO4 (đậm đặc) = 4I2 + H2S + 4H2O
Khi nồng độ H2SO4 thay đổi thì chất tạo thành có thể khác nhau như:
Zn + 2H2SO4 (đậm đặc) = ZnSO4 + SO2 ↑ + 2H2O
3Zn + 4H2SO4 (đậm đặc) = 3ZnSO4 + S + 4H2O
4Zn + 5H2SO 4 (đậm đặc) = 4ZnSO4 + H2S ↑ + 2H2O
Phản ứng với kim loại
Axit sunfuric đậm đặc ở nhiệt độ thường có thể tác dụng với các kim loại mạnh như sắt và nhôm. Khi đun nóng, axit sunfuric đậm đặc có thể phản ứng với tất cả các kim loại (bao gồm vàng và bạch kim) ngoại trừ iridium và ruthenium để tạo thành muối kim loại hóa trị cao.
Cu + 2H2SO4 (đậm đặc) -> CuSO4 + SO2 ↑ + 2H2O
Phản ứng phụ:
5Cu + 4H2SO4 (cô đặc) -> 3CuSO 4 + Cu2S + 4H2O
Tác dụng với sắt III tạo khí CO2, nước và muối sắt.
2Fe + 6H2SO4 (đậm đặc) -> Fe2(SO4)3 + 3SO2 ↑ + 6H2O
Phản ứng với phi kim
Axit sulfuric đậm đặc có thể ôxi hóa phi kim như carbon, lưu huỳnh, phốt pho…Trong loại phản ứng này, axit sunfuric đậm đặc chỉ thể hiện tính chất oxy hóa.
C + 2H2SO4 (đậm đặc) -> CO2 + 2SO2 ↑ + 2H2O
S + H2SO4 (đậm đặc) -> 3SO2 ↑ + 2H2O
2P + 5H2SO4 (đậm đặc) -> 2H3PO4 + 5SO2 ↑ + 2H2O
Phản ứng với các chất khử khác
Ngoài khả năng phản ứng với kim loại, phi kim thì nó còn có thể tác dụng với hydro sunfua , hydro bromua , hydro iodua.
H2S + H2SO4 (đậm đặc) -> S ↓ + SO2 + 2H2O
2HBr + H2SO4 (đậm đặc) -> Br2 + SO2 + 2H2O
8HI + H2SO4 (đậm đặc ) -> 4I2 + H2S + 4H2O
CaF2 + H2SO4 → CaSO4 + 2HF
Tính chất hóa học của Axit Sunfuric loãng
Axit sunfuric làm chuyển màu quỳ tím hóa đỏ.
+ H2SO4 tạo thành muối sunfat khi tác dụng với kim loại đứng trước H (trừ Pb)
Fe + H2SO4 → FeSO4 + H2
+ H2SO4 tạo thành muối mới khi tác dụng với oxit bazơ (trong đó kim loại giữ nguyên hóa trị) và nước .
FeO + H2SO4 → FeSO4 + H2O
+ H2SO4 tạo thành muối mới axit sunfuric tác dụng với muối (trong đó kim loại vẫn giữ nguyên hóa trị) và axit mới.
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2
H2SO4 + 2KHCO3 → K2SO4 + 2H2O + 2CO2
+ H2SO4 tạo thành muối mới và nước khi axit sunfuric tác dụng với bazơ.
H2SO4 + NaOH → NaHSO4 + H2O
H2SO4 + 2NaOH → Na2SO4 + 2H2O
Phương trình điều chế H2SO4
FeS2 hoặc S → SO2 → SO3 → H2SO4
+ Đốt cháy quặng firit sắt:
4FeS2 + 11O2 → 8SO2 + 2Fe2O3
+ Oxi hóa SO2 bằng oxi trong điều kiện 400 – 500 độ C, xúc tác V2O5):
2SO2 + O2 → 8SO3
+ Axit sunfuric đặc hấp thụ SO3 tạo thành oleum có công thức tổng quát là H2SO4.nSO3:
nSO3 + H2SO4 → H2SO4 .nSO3
+ Pha loãng oleum thành axit sunfuric bằng lượng nước thích hợp:
H2SO4 .nSO3 + (n+1) H2O→ (n+1)H2SO4